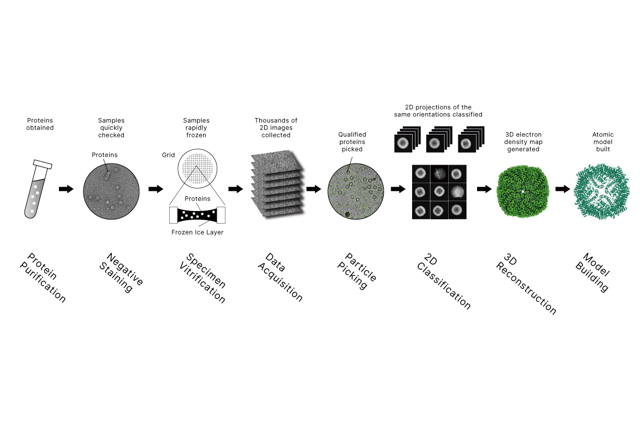
ChIP:タンパク質が遺伝子を制御する方法を明らかにする:一つのシンプルな問いから始まります
2026-02-25ChIP: Revealing How Proteins Control Genes is the practical method scientists use to answer a question that sits at the center of modern biology: which proteins are sitting on which DNA regions, in real cells, under real conditions? If you are new to gene regulation, it helps to think of DNA as a library and regulatory proteins as "readers" that open specific pages at specific times. ChIP (Chromatin Immunoprecipitation) is how we capture that moment and identify the pages.
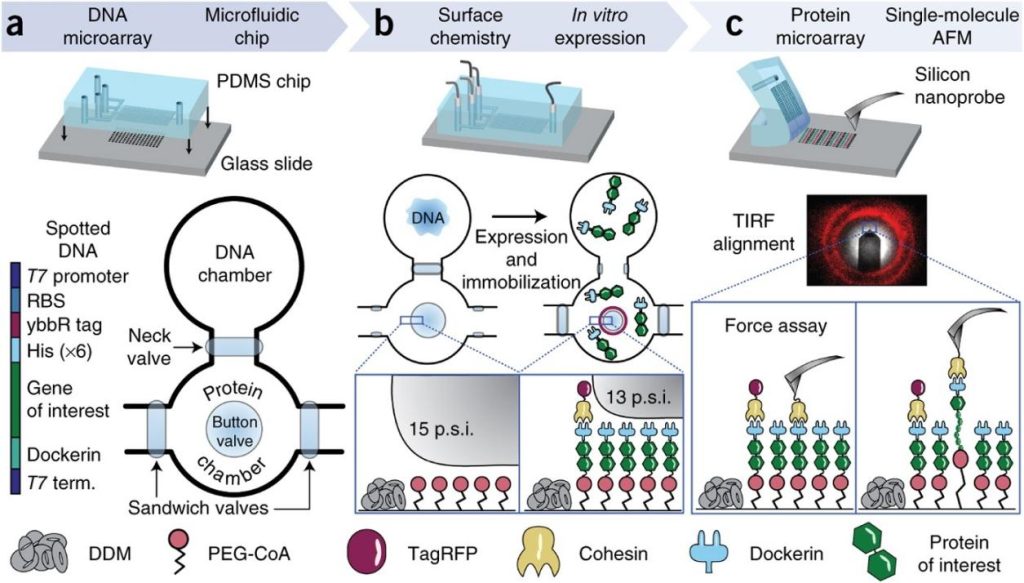
遺伝子からチップ上のタンパク質力学へ |ネイチャー・メソッド
Longlight Technologyでは、クロマチン研究で使用されるコアワークフローツールを製造・サポートしています。サンプル取り扱いの必須から濃縮、下流検出オプションまで、新規チームがクリーンで再現可能な経路からスタートでき、経験豊富なチームも自信を持ってスケールできます。
ChIPが実際に何を測定し、なぜ重要なのか
率直に言えば、 欠く tests whether a protein is physically associated with a specific DNA region inside the cell. It is widely used for transcription factors, co-factors, and histone modifications, because these are the "switches" that decide whether genes are active, paused, or silent. A standard ChIP workflow usually includes crosslinking (for many targets), chromatin fragmentation, antibody-based enrichment, DNA purification, and readout by qPCR (targeted) or sequencing (genome-wide).
だからこそ、ChIP:タンパク質制御の方法を明らかにする」は単なる実験技術以上のものであり、意思決定ツールなのです。研究者の助けとなる:
✓ 疑わしい調節因子が促進剤または強化剤に結合するかどうかを確認する
✓ 治療前後の結合変化を比較する
✓ 活性または抑制されたクロマチン状態と相関するマップヒストンマーク
✓ エピジェネティクス、腫瘍学、免疫学、発生におけるメカニズムのエビデンスを構築する
6ステップのコアワークフロー
Most beginners succeed faster when they treat ChIP as a chain of "must-not-break" steps, not as one single experiment. Here is the practical sequence behind ChIP: Revealing How Proteins Control Genes:
・固定(オプションですが一般的な):多くのChIPプロトコルでは可逆架橋が用いられ、多くの場合1%ホルムアルデヒドを~10分間使用し、その後(一般的にグリシンで)焼却します。
・溶解/クロマチン調製:核/クロマチンの収率を一貫性のために標準化する。
・DNA剪断:断片化が分解と濃縮速度を制御します。
・免疫沈殿:抗体特異性がS/Nの主な決定因子です。
• 架橋逆転(使用された場合)およびDNA精製:高い純度はアッセイ感度を高めます。
• 読み上げ:焦点を絞った質問にはChIP-qPCR、ゲノム全体マッピングにはChIP-seqを使用します。
Longlight Technology CTA:初めてChIPワークフローを構築する場合は、ターゲットタイプ(TF対ヒストンマーク)および読み出し計画(qPCR対シーケンス)に合わせた開始から終了までのチェックリスト(サンプルからデータへの順)を当チームにご連絡ください。
断片化と架橋:結果を左右する二つの環境
If your ChIP results feel "random," the root cause is often upstream. Two settings dominate reproducibility:
強度と時間の交差。重架橋は弱い相互作用を安定化させることができますが、DNA収量を減らし、下流の工程を複雑にすることもあります。多くの標準プロトコルでは、1%ホルムアルデヒドを、約10〜15分などの短い室温培養ウィンドウで使用し、その後焼光を行っています。
断片サイズ。ほとんどのChIPアプリケーションでは、一般的に推奨される剪断範囲は~200〜600 bpであり、細胞タイプや組織を超えた分解能と回復可能性のバランスが取れています。
✓ 大きすぎる(例:>800〜1000 bp)は解像度を低下させ、背景を増加させることが多いです
✓ 小さすぎるとエピトープを損傷し、回収可能なDNAの低下、バイアスライブラリーを損傷する恐れがあります
✓ The "best" settings are instrument- and sample-dependent, so optimization is normal, not a failure
これがChIP:タンパク質がどのように遺伝子を制御するかを明らかにする隠れた真実です:最もクリーンな下流解析では、不整合なクロマチン前製を救うことはできません。
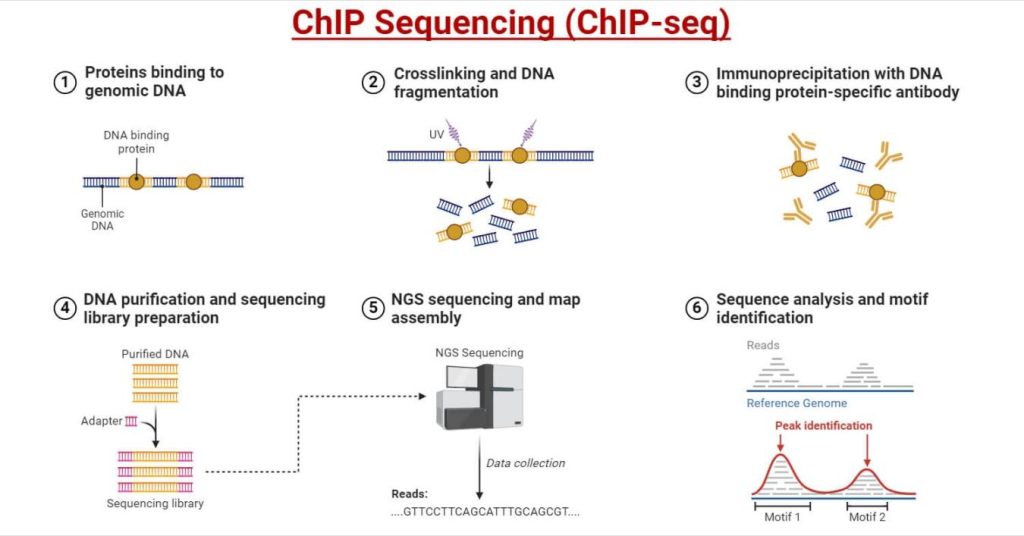
ChIPシーケンス(ChIP-seq):原理、ステップ、用途、図解
Antibodies, Controls, and What "Good Enrichment" Looks Like
ChIPは抗体駆動型アッセイなので、ターゲット抗体とコントロールがデータの信頼性を決定します。
初日から計画すべきコントロール:
✓ 回復を正規化するためにDNA(IP前のクロマチンの一部)を入力
✓ 非特異的なプルダウン背景を測定するためのIgGコントロール
✓ システムが正常に動作していることを確認するための既知の陽性遺伝子座(利用可能な場合)があります
現実的な濃縮の期待値はターゲットタイプによって異なります。例えば、一部の医療提供者は、転写因子/補因子のChIP濃縮が総入力の~0.5%と低くなることがある一方で、ヒストン修飾によるChIPはマークの存在比や抗体の性能に応じて劇的に高く(数十パーセント)と報告されています。ビーズを用いた典型的なIgG背景は入力の約~0.05〜0.1%程度です。
That range is not meant to intimidate you—it is meant to protect you from false expectations. In ChIP: Revealing How Proteins Control Genes, "small" can still be correct, as long as it is specific, reproducible, and above background with proper controls.
Longlight Technology CTA:高バックグラウンド信号や弱信号のトラブルシューティングをお考えの場合は、制御設計テンプレート(プライマー戦略、入力割画計画、バックグラウンド閾値)をご依頼ください。ボトルネックを迅速に診断できるようにしてください。
ChIP-qPCRとChIP-seq:目標に合った適切な読み取り方法の選択
A beginner-friendly rule is: qPCR answers "Is it there?" while sequencing answers "Where else is it?"
ChIP-qPCRは、少数の疑われる領域(プロモーター/エンハンサー)があり、迅速な反復が必要な場合に理想的です。また、シーケンシングに投資する前の実用的なステップでもあります。
ChIP-seqは発見やゲノムワイドマッピングに最適ですが、深さや品質指標の計画が必要です。ENCODEガイダンスは、以下のようなよく参照されるターゲットを提供します:
転写因子/狭ピーク実験の場合:1回の複製あたり最低~1,000万個の利用可能な断片を持ち、推奨ターゲットは高めです。
広範なヒストンマークの場合:1回の複製あたり最低~2,000万個の利用可能な断片を持ち、目標に応じて推奨される標的は高めです。
These numbers are not just "sequencing advice." They shape how much starting material you need, how strict your antibody must be, and how carefully you must manage batch effects. That is why ChIP: Revealing How Proteins Control Genes is often won or lost at the design stage.
QubitアッセイチューブとChIP-Seqサービスの利点:一つのワークフロー、一つの標準
サンプルからレポートへ
ChIP: Reveing How Proteins Control Genesを実際の研究スケジュールに適用するためには、サンプルの摂取から最終解釈までワークフローが一貫していなければなりません。Longlight Technologyは、Qubit Assay Tubesのような信頼できる消耗品と、ハンドオフの削減、変動の制御、初心者から経験豊富なチームまで結果の読みやすいエンドツーエンドのChIP-seqサービスと組み合わせています。
ボトルネックを解消するワンストップサービス
当社のサービスモデルは、完全なシーケンスパイプラインを社内で構築せずにChIP-seqの結果を求めるラボ向けに設計されています。固定細胞サンプルや凍結組織サンプルを提供し、残りのステップは標準化されたチェックポイントで完了します。
✓ サンプル準備および受理 QC
✓ クロマチン剪断および断片化制御
✓ 図書館建設および図書館品質管理
✓ 機器上のシーケンスおよびデータ品質管理
✓ バイオインフォマティクス分析および構造化報告
✓ 完全なレポートおよび生データの提供
すべてのリンクで厳格な品質検査を実施
ChIP-seqは信号対雑音比(CMP)性能に依存します。取り扱い、せん断、ライブラリの指標における微妙なプロセスの変動は、真の信号を希釈することがあります。Longlight Technologyは全体を通じて厳格な品質管理を導入し、自信のある濃縮と明確な結合解釈を可能にします。
✓ 再現性を保護するための段階的な品質管理
✓ 実験的QCと下流解析を整合させるデータ品質チェック
✓ 特定の遺伝子や領域での結合をより信頼して特定できるクリーンな報告
小規模サンプルサイズに適しています
多くの研究チームは、特に一次細胞、希少組織、初期サンプルの研究において、限られた資料で作業しています。最適化された実験フローは、サンプル入力が制限されていてもChIP-seq実験と解析を完了できるよう設計されています。
✓ 低投入プロジェクトのプロセス最適化
✓ Practical design guidance to avoid "rework loops" caused by insufficient QC
✓ 小サンプル研究を解釈可能に保つための安定したワークフロー
ターゲットを絞った質問:特定の遺伝子や領域、またはゲノム全体の発見
ChIPは、実際のクロマチン文脈を反映した形でタンパク質–DNA相互作用を研究します。ChIP-seqは、ChIPと次世代シーケンシングを組み合わせ、ゲノム全体で特定の転写因子やヒストンによって結合したDNA部位を検出します。目標に応じて、私たちの分析は集中型と発見型の両方の研究を支援できます。
ChIP-seqは以下の質問に答えるのに役立ちます:
✓ タンパク質が部位間でどこに現れ、ターゲットゲノム領域で結合をマッピングするかを比較します
✓ ヒストン修飾パターンが遺伝子発現変化とどのように関連しているかを探る
✓ RNAポリメラーゼIIおよびその他のトランスファクター結合部位の正確な位置を特定する
✓ 結合と調節結果を結びつけるための転写因子の研究
ロングライトテクノロジーを選ぶ理由
ロングライト・テクノロジーは、実用的な製品・サービスエコシステムを通じて現代ゲノミクスを支援しています。ChIP-seqサービスに加え、焦点超音波計などのNGS関連機器や、学術、臨床、産業現場で使用される高品質な試薬や消耗品も提供しています。
✓ 消耗品およびキット:プレキャストアガロースゲル、核酸スカベンジャー、キュービットチューブ、核酸抽出キット、ライブラリー準備キット
✓ ゲノミクスソリューション:ラボの効率、精度、再現性を向上させるために設計された製品
✓ リサーチサポート:サンプルから有用な結論へチームが進むのを支援するワークフローガイダンス
最終要点
ChIP:『タンパク質の制御方法』は、コントロールされたシステムとして扱うときに最も効果的です。安定したクロマチン準備、検証済みの抗体、正直な対照、そしてあなたの質問に合致する指標です。その論理でワークフローを構築しれば、ChIPは現代の研究室で使える遺伝子調節の最も明確な窓口の一つになります。
もしよければ、ターゲットタイプ(TF対ヒストンマーク)やサンプル形式(細胞対組織)を共有していただければ、初心者向けのワークフローチェックリストとQCポイントをあなたのユースケースに合ったものを、同じ明快で読みやすいスタイルでまとめます。