関連記事
クリオEM:ほぼ原子分解能で生体分子を可視化する
2026-02-21Cryo-EM:生体分子を原子分解能に近いレベルで可視化することは、構造生物学を再構築しています。なぜなら、研究者が結晶や過度なサンプル取り扱いを要求することなく、現実に近い条件下でタンパク質、複合体、ウイルスを観察できるからです。Longlight Technologyは、明確なワークフロー、透明な成果物、実践的なガイダンスを備えたクライオ電子顕微鏡プロジェクトを支援し、チームが「有望なサンプル」から「防御可能な構造」へとより速く、行き止まりを減らすのを支援します。
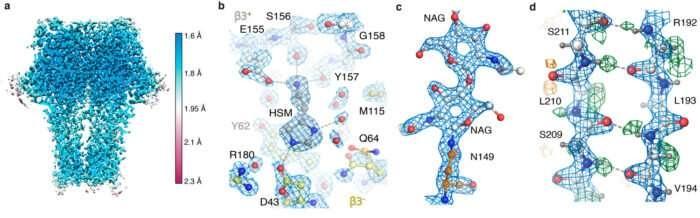
科学者たちは単一粒子のクライオEMで個々の原子を可視化するために解像度の記録を破る
クライオEMを完璧なサンプルにしか機能しない神秘的でハイエンドなサービスとして扱うのではなく、構造化された意思決定システムとして捉えています。つまり、持っているものをスクリーニングし、その動きを学び、サンプルが本当に準備できたときにのみ高解像度データ収集にスケールアップします。その考え方は時間、予算、貴重な資料を節約します。特に、内部レビューやピアレビューを通過できる結果を必要とする初めてのユーザーにとってはなおさらです。
なぜ低温電磁波が現代構造生物学に重要なのか
クライオEMとは何か
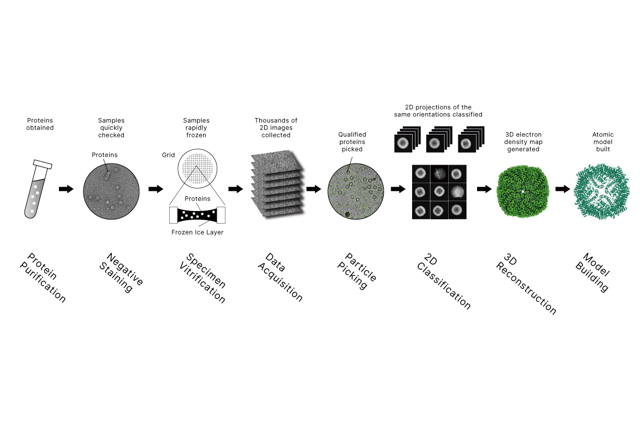
クライオEM(クライオ電子顕微鏡) は、生物分子をガラスのような薄い氷層で急速に凍結した後、電子顕微鏡でイメージングすることで「観察」する方法です。凍結は化学的固定や結晶化なしに分子をほぼ本来の状態にロックし、コンピュータは多くの2Dビューを組み合わせて3D構造を再構築します。これはよく動作するサンプルに対しては原子レベルの解像度に近いものが多いです。
クライオEMの仕組み(シンプルビュー)
・サンプル(タンパク質、複合体、ウイルスなど)を溶液中で準備します
・急速凍結で水をガラスのような氷(氷の結晶なし)に変える
・透過電子顕微鏡を用いて数千から数百万の粒子を画像化
・計算:3Dマップの整列、分類、再構築;時には原子モデルを構築することもあります
主な低温EM手法
・単一粒子分析(SPA):精製されたタンパク質/複合体に最適;ここでは最高解像度がよく使われます。
・クライオ電子断層撮影(Cryo-ET):細胞や自然環境内の構造の3Dイメージング;空間的な文脈にとても役立ちます。
・マイクロ電子回折(MicroED):結晶構造が難しい場合に非常に小さな結晶(ナノ/微小結晶)に対して。
なぜ人々がCryo-EMを選ぶのか
•結晶を育てる必要はありません
・分子の本来の状態に近いものを捕捉する
・大規模な複合体や多くの「難しい」ターゲットに有効です
・複数の構造状態(運動/柔軟性)を明らかにできる
生命科学において、生体分子を理解する最も速い方法は、その形状とその変化を見ることです。クライオEMは、困難で柔軟、不安定なターゲット、つまり多くのチームが最も重視するターゲットに対してこれを可能にします。低温電子顕微鏡は透過電子顕微鏡を基盤とし、試料の挙動やデータ品質に応じて、サブナノメートルからほぼ原子レベルの3D構造を再構築できます。
これは特に、詳細が意思決定を左右する高インパクト分野において重要です。
・創薬:結合ポケット、界面形状、誘導適合変化
・抗体とワクチン:エピトープマッピング、中和機構、複雑な安定性
・ウイルス学:カプシド組織、立体構造の変化、アセンブリ経路
•膜タンパク質:チャネル、トランスポーター、受容体、多重通過複合体
多くの現代のターゲットは簡単には結晶化せず、中には結晶しないものもあります。クリオEMは「結晶化が難しい」と「今はテスト可能」に変換することが多いです。なぜならワークフローは反復を前提に作られているからです。素早くスクリーニングし、条件を賢く調整し、粒子が反応したらスケールアップします。
クライオEMとX線結晶構造:初心者が知っておくべきこと
X線結晶学は依然として強力な手法であり、適切な場合には非常に高い分解能に達することができます。しかし、構造生物学のプロジェクト計画が初めてなら、理論的な最大分解能だけでなくリスクと確率に注目するのが役立ちます。
クライオEMは、いくつかの一般的なプロジェクトの障害を軽減します。
・結晶化が不要で、大きな不確実性が除去されます
・ガラス化した氷にほぼ原生状態を保存し、生物学的関連性を高める
・柔軟なターゲットや動的なターゲットは「平均化される」のではなく評価可能です
•ハードターゲット(膜タンパク質、大型アセンブリ、ウイルス)がより実現可能になる
・異質性は時に計算的に異なる状態に分離されることがあります
・早期発見サンプル(ケース依存)では純度許容度の低さが可能になる場合があります
・繰り返し結晶化スクリーニングと比較して試料廃棄物が少ない
簡単に考えると、結晶学は結晶化がうまくいく場合に驚異的ですが、難しいターゲットや多成分複合体、試行錯誤が難しいプロジェクトでは、クライオEMの方が予測しやすいことが多いのです。
X線結晶構造学、NMR、電磁気象の比較 - 創造的生体構造
私たちが提供する構造的解決策:スクリーニングから準原子モデルまで
Longlight Technologyでは、私たちのクライオEMサービス構造は実際のプロジェクトの進行に合致しています。私たちは作業を3つの実践的な目標にまとめています。つまり、あなたの進路がサンプルと答えたい問いに合致するようにしています。
陰性染色スクリーニングによるサンプル適合性評価
低温グリッドや高性能顕微鏡の時間に投資する前に、ネガティブステインスクリーニングは現実確認の役割を果たします。通常は室温で行われ、まず重要な疑問に答えるのに役立ちます。すなわち、試料は構造試料のように振る舞うかどうかです。
ネガティブステインは以下のことを明らかにします:
•集約または凝集
・粒子の完全性と形態
・サイズ分布と濃度適合性
•粗雑な異質性(同時にあまりにも多くの「形状」を持つ)
・不安定性や劣化の兆候
ネガティブステインは品質ゲートのようなものだと考えてください。高解像度地図の公開を目的としたものではありません。これは、未準備のサンプルに対する高額なデータ収集を避け、推測ではなく証拠を用いて次の最適化ステップを導くことを目的としています。
単一粒子解析による高分解能構造決定
多くの可溶性タンパク質や複合体において、単一粒子解析(SPA)が高分解能の結果を得る最も一般的な方法です。大規模なデータセットには、さまざまな向きからの個別のパーティクルビューが含まれています。計算処理はこれらの粒子画像を整列・分類し、3D密度マップを再構築します。地図がそれを支持すれば、原子モデルを構築し、洗練させて生化学的読み取りだけでは見えないメカニズムを明らかにすることができます。
SPAは、Cryo-EM: Visualizing Biomocules at Near-Atomic Resolution(原子分解能に近い形で生体分子を可視化する)が直接実践可能になる場であり、結合界面、ドメインの移動、活性、阻害、特異性の構造的説明を自信を持って記述できます。
凍結電子断層撮影による現地構造解析
もし質問が「この精製された粒子はどのような姿か」ではなく、「文脈の中でどのように組織されているか」であれば、クライオ電子断層撮影(Cryo-ET)の方が適しています。トモグラフィーはよりネイティブな環境で構造を可視化できるため、以下の用途に役立ちます:
•膜関連アセンブリ
•大規模な細胞複合体
・ウイルスと宿主の相互作用組織
・空間配置と建築に関する質問
クライオETは、分子形状と同じくらい空間的な物語が重要な場合に選ばれます。
私たちのサービスワークフローと、あなたが受け取るもの
クリオEMプロジェクトはブラックボックスのように感じるべきではありません。各段階に明確さを組み込み、何が起きているのか、何が観察され、どんな決定がなされているのかを常に把握できるようにしています。
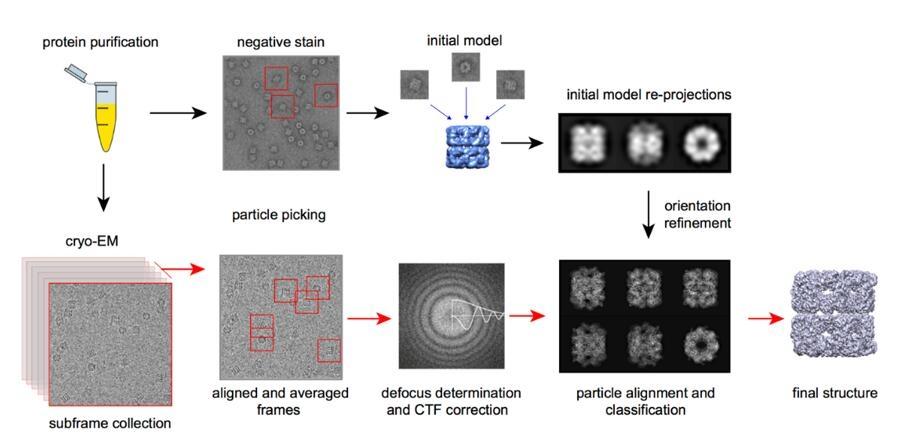
典型的なワークフロー:
プロジェクト協議→NDA署名→サービス契約、サンプル受領→確認、→品質検査→陰性染色スクリーニング→低温EMデータ収集→データ処理→報告書の提出
納品物は「良い写真」のためだけでなく、実際の研究用途のために構成されています。範囲に応じて、以下を受け取ることができます:
・生のクライオEMムービー(該当する場合はゲイン参照ファイル付き)
•主要な中間処理出力
・解像度と品質指標を含む最終的な3D密度マップ
・原子座標モデル(密度がモデル構築を支持する場合)
・検証およびクロスチェック報告(例:構造品質評価)
• 安全なクラウドまたはポータブルストレージによる組織的なデータ配信
目標はシンプルです。必要なら再加工し、自信を持って出版できるようにすることです。後でファイルを追いかけたり、結論の至り方を考えたりする必要がないのです。
異なるプロジェクト段階に合わせた機器プラットフォーム
サンプルによって必要な楽器のパワーや戦略のレベルも異なります。基本的なスクリーニング質問に答えるために旗艦システムにお金を払うのは非効率的で、プロジェクトの進行を遅らせることが多いです。
当社のクライオEMサービス機能は、高解像度構造決定をカバーするプラットフォームによって支えられています。例えば:
・Talos L120C G2:効率的なTEM/クライオEMスクリーニングと評価
•グラシオス2(200 kV):ルーチンのSPAおよびクライオETワークフローに強力な働き者システム
・Titan Krios G4(300 kV):安定性、自動化、スループット、そして最高解像度の可能性を重視したフラッグシッププラットフォーム
この段階的なアプローチは実践的な原則を支えています。それは、適切な瞬間に適切な顕微鏡を使うことです。スクリーニングは効率的であり、高解像度の採取はサンプルが正当化できる準備ができたときにのみ行われます。
実践的なプロジェクト要件、納品期間、そして明確な次のステップ
初めての構造プロジェクトを計画している場合、サンプル準備の詳細が重要です。ほとんどの遅延は「顕微鏡」によるものではなく、不安定性、集積、または互換性のないバッファ成分といった回避可能なサンプルの問題によって引き起こされます。
典型的な最小サンプルガイダンス:
・ネガティブステイン:~1 g/L、~100 μL
•SPA(可溶性タンパク質):~1 g/L、~100 μL
•SPA(膜タンパク質):~1 g/L、~100 μL(多くの場合、議論で調整可能)
典型的なバッファ誘導:
•pH 6.0–8.5
・塩分濃度<200 mM
・低グリセロールおよび低アジドを好みます(ケースバイケース最適化可能)
典型的な納品期間:
・陰性染色スクリーニング:1〜2週間
・SPAの予備的アウトカム:6〜8週間
・SPA高解像度モデル(可能の場合):~2〜3ヶ月
CTA:新しいターゲットのリスクを迅速に減らしたいなら、まずはネガネージステインスクリーニングから始めてください。Longlight Technologyにサンプルの詳細(ターゲットタイプ、バッファー、濃度、推定純度)を送っていただければ、科学的目標とスケジュールに応じて、最も効率的な方法—ネガ・ステイン、SPA、またはクライオET—を提案します。
最後に、多くのクライオEM研究は上流および下流の生物学に関連しています。Longlight Technologyは、焦点超音波検査などのNGS関連機器や、一般的に使われる消耗品やキット(プレキャストアガロースゲル、核酸抽出キット、ライブラリー調製キット)を含む、より広範な分子生物学およびゲノミクスのワークフローもサポートしており、構造作業が発見、検証、論文準備の研究設計にスムーズに結びつくようにしています。